استفاده از ابررایانهها برای کشف رازهای ترمیم DNA
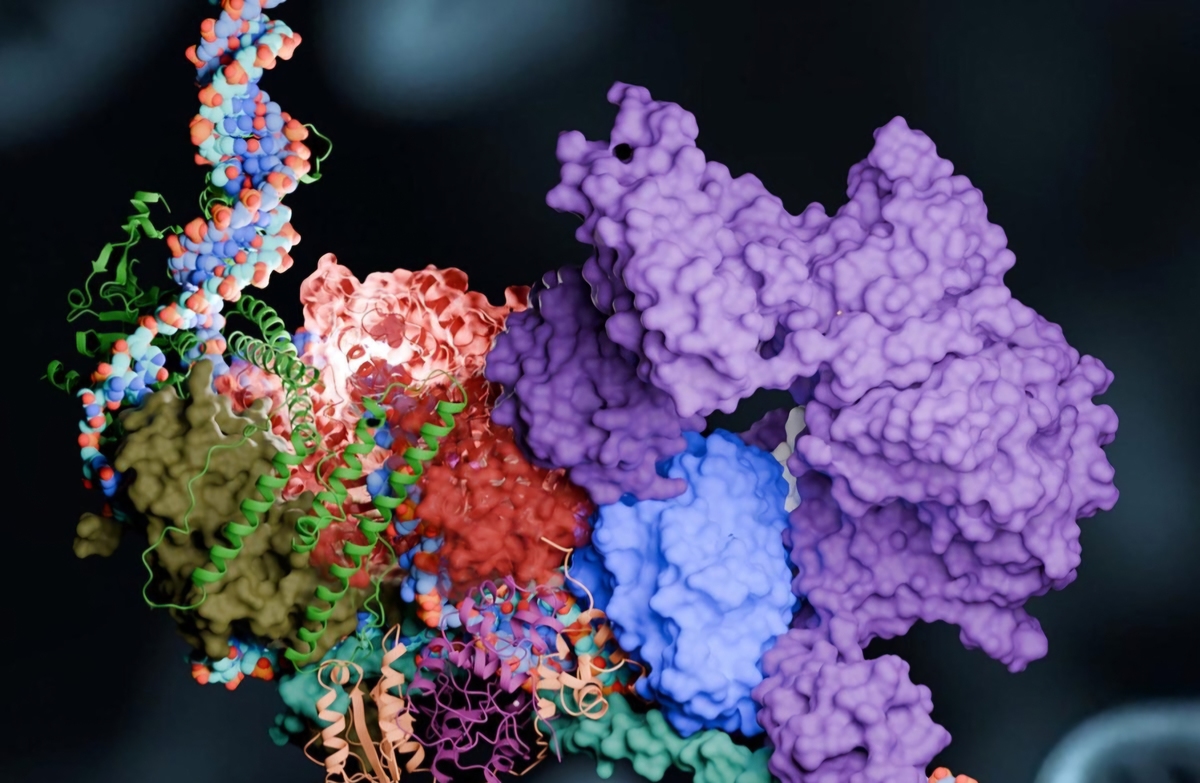
محققان از قدرت پیشرفتهترین ابرکامپیوترهای جهان برای شبیهسازی نحوه عملکرد ماشینآلات سلولی که DNA را ترمیم میکنند و به پیشگیری از بیماریهای تهدیدکننده زندگی کمک میکنند، بهره بردهاند.
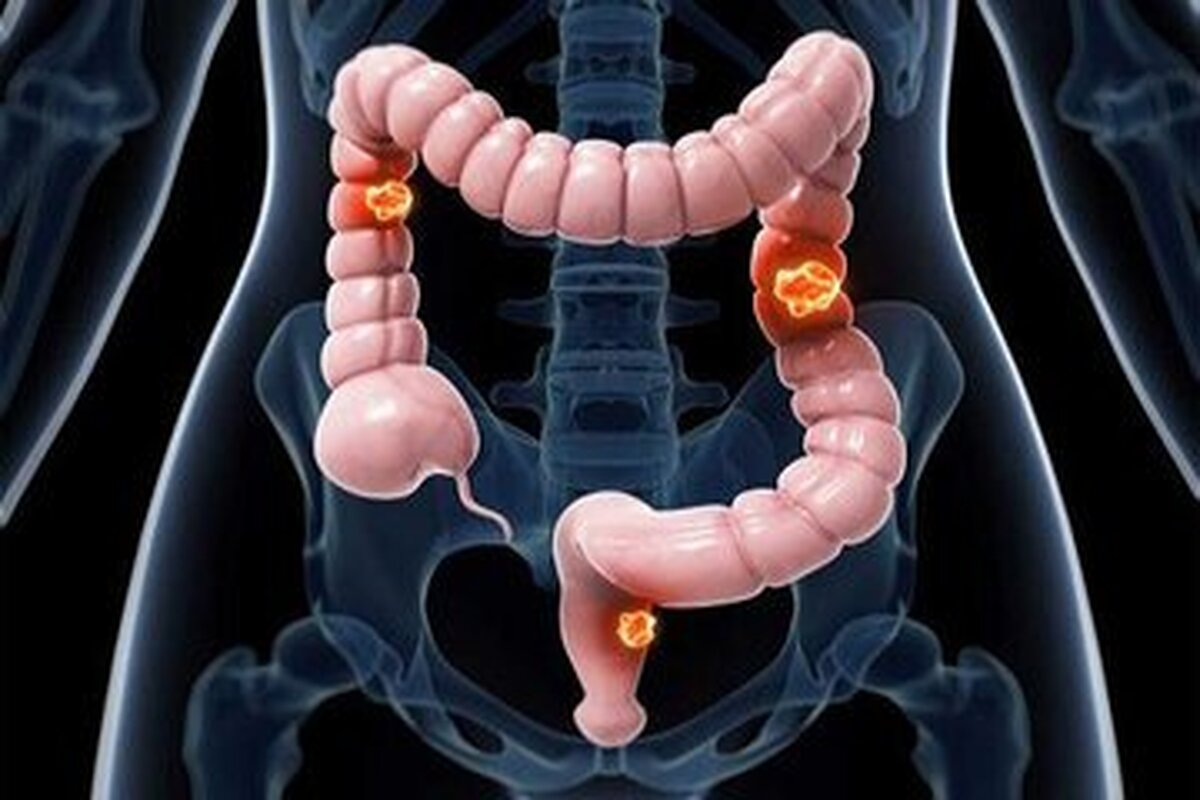
آفتابسوختگی و پیری زودرس از جمله عواقب شناخته شده قرار گرفتن در معرض تابش اشعه ماوراء بنفش (UV)، دود تنباکو و سایر سرطانزاها هستند. اما آسیبها تنها به سطح بدن محدود نمیشوند؛ در داخل بدن، این عوامل مضر میتوانند DNA را به طور واقعی پاره کنند.
به گزارش ساینس دیلی، درک نحوه ترمیم و محافظت بدن از این آسیبهای DNA برای پیشرفت درمانهای اختلالات ژنتیکی و بیماریهای تهدیدکننده زندگی مانند سرطان بسیار حیاتی است. با این حال، علیرغم پیشرفتهای قابل توجه در تحقیق و پزشکی، بسیاری از جنبههای مکانیزمهای مولکولی پشت ترمیم DNA هنوز بهطور کامل درک نشدهاند.
برای روشنتر کردن این فرآیند، محققان دانشگاه ایالتی جورجیا در چند سال گذشته از ابرکامپیوتر Summit در آزمایشگاه ملی اوک ریج وزارت انرژی ایالات متحده استفاده کردهاند. تمرکز آنها بر روی مکانیزم پیچیدهای از ترمیم DNA به نام ترمیم خروج نوکلئوتیدی (NER) است. این مسیر به مجموعهای هماهنگ از ترکیبهای پروتئینی وابسته است که آسیب DNA را با دقت شگفتانگیزی شناسایی و حذف میکنند.
در آخرین مطالعه خود که در مجله Nature Communications منتشر شد، تیم تحقیقاتی مدل کامپیوتری دقیقی از یکی از اجزای کلیدی NER به نام مجموعه پیش-incision (PInC) توسعه داده است. PInC نقش مهمی در تنظیم ترمیم DNA در مراحل بعدی مسیر NER ایفا میکند. با کشف نحوه عملکرد PInC و جایگاه آن در فرآیند ترمیم، محققان امیدوارند اهداف درمانی جدیدی برای درمان سرطان و پیشگیری از بیماریهای مرتبط با آسیب DNA و پیری زودرس پیدا کنند.
ایوایلو ایوانوف، استاد شیمی در دانشگاه ایالتی جورجیا و محقق اصلی این پروژه گفت: "ما به نحوه ترمیم مواد ژنتیکی سلولها علاقهمند هستیم. NER یک مسیر چندمنظوره است که انواع مختلف آسیبهای DNA را با استفاده از یک فرآیند سهمرحلهای ترمیم میکند که به ماشینآلات مولکولی دقیقاً متعادل متکی است. متاسفانه، جهشهای مضر میتوانند توسعه یابند که این ماشینآلات را مختل کرده و موجب بیماریهای شدید انسانی شوند. "
وی افزود: "با این حال، اثرات جهشهای ژنتیکی میتوانند بسته به موقعیت آنها در داخل پیچیدههای ترمیم به طرز چشمگیری متفاوت باشند. در برخی موارد، جهشها باعث حساسیت به نور UV و تمایل شدید به سرطان میشوند. در موارد دیگر، این جهشها موجب رشد غیرطبیعی و پیری زودرس میشوند، اما چرا این اتفاق میافتد هنوز بهطور کامل در سطح مولکولی درک نشده است. این معما هدف تلاشهای مدلسازی کامپیوتری ما است.
سه مرحله ترمیم
فرآیند NER در سه مرحله متمایز صورت میگیرد: شناسایی، تأیید و ترمیم. هر مرحله نیاز به گروههای مختلفی از پروتئینها دارد تا عملکردهای خاص خود را انجام دهند، درست مانند یک تیم اورژانس که متخصصان مختلفی برای درمان بیماران آسیبدیده در اختیار دارد. به همین ترتیب، ماشینآلات NER میتوانند بسته به وظیفهای که در پیش دارند شکل خود را تغییر دهند.
در مرحله اول، پروتئین NER به نام XPC (گروه Xeroderma Pigmentosum C) بهعنوان یک امدادگر اولیه عمل کرده و محل آسیبدیدگی DNA یا لزیشن را شناسایی کرده و سپس هلیکس DNA را بهطور خاص پیچیده میکند تا آسیب در دسترس قرار گیرد. XPC سپس پروتئینهای دیگر را برای کمک به شروع مرحله دوم، یعنی تأیید آسیب یا اسکن لزیشن، فرا میخواند.
در این مرحله، ماشینآلات پروتئینی NER به شکل بعدی خود تغییر مییابند. وقتی XPC کنار میرود، مجموعه پروتئینی به نام فاکتور رونویسی IIH (TFIIH) وارد عمل میشود و قسمت DNA را بیشتر باز کرده و رشته جدید را برای یافتن آسیبها اسکن میکند.
بعد از آن، این نوبت جراح است — یعنی PInC — که در مرحله سوم و نهایی ترمیم عمل کند.
ترمیم نهایی
با تثبیت و آمادهسازی "بیمار" برای جراحی، عملیات حذف رشته آسیبدیده DNA آغاز میشود. دو آنزیم، XPF و XPG (گروههای F و G از Xeroderma Pigmentosum)، دقیقاً در هر دو طرف لزیشن قرار گرفته و بهعنوان قیچیهای مولکولی عمل کرده و بخش آسیبدیده DNA را بریده میزنند.
پس از حذف لزیشن، DNA جدید برای پر کردن شکاف باقیمانده سنتز میشود. در نهایت، ستون فقرات DNA بسته میشود و DNA آسیبدیده به حالت طبیعی خود باز میگردد.
ایوانوف افزود: "آنچه ما میخواهیم بدانیم این است که چگونه PInC پس از مرحله اسکن لزیشن تشکیل میشود. چگونه این مرحله موقعیت دو زیرواحد آنزیمی را که بریدن دوگانه رشته آسیبدیده DNA را انجام میدهند، کنترل میکند؟ و بهطور مهم، آیا بین این دو آنزیم ارتباطی وجود دارد؟ آیا آنها یکدیگر را حس میکنند؟ "
این موضوع اهمیت دارد، زیرا هنگامی که رشته آسیبدیده DNA بریده میشود، ضروری است که فرآیند ترمیم با پر کردن آن شکاف تکمیل شود. در غیر این صورت، منجر به مرگ سلولی یا ایجاد شکستهای دو رشتهای میشود که برای سلول بسیار مضر هستند.
شبیهسازیهای نهایی
برای پاسخ به این سؤالات، محققان ساختار PInC را حل کردند. در زیستشناسی، درک ساختار پروتئین برای درک رفتار یا عملکرد تجمعات پروتئینی بسیار ضروری است. اشکال، اندازهها و تعاملات پروتئینها تعیین میکنند که چگونه آنها به هم پیوسته و تجمعات بزرگ بیومولکولی را تشکیل میدهند.
محققان از مدل پیشرفته AlphaFold۲ برای پیشبینی ساختارهای ناشناخته و رابطهای میان پروتئینها استفاده کردند. در نهایت، شبیهسازیهای دینامیک مولکولی با استفاده از کد NAMD بر روی ابرکامپیوتر Summit که قادر به انجام ۲۰۰ هزار تریلیون محاسبه در هر ثانیه است، انجام شد.
محققان با شبیهسازیهای گسترده توانستند اطلاعات زیادی در مورد پیچیدگی PInC بدست آورند. نتایج این تحقیق میتواند به فهم بهتر بیماریهای ژنتیکی کمک کند که بهطور عمده ناشی از جهشهای در پروتئینهای XPF و XPG هستند.
در پایان، ایوانوف و تیمش قصد دارند از ابرکامپیوتر Frontier که جانشین Summit است برای بررسی مسیر NER وابسته به رونویسی استفاده کنند.
این تحقیق با حمایت مرکز محاسبات علمی پیشرفته انجام شده است.
انتهای پیام/